Скорость нарастания льда в зависимости от температуры. ледостав и поведение на тонком льду
Содержание:
- Замерзание водоёмов
- Свойства
- Модель строения воды
- Структура и деформации ледяною покрова.
- Правильное хранение сухого льда
- Как определить толщину для рыбалки?
- Правила передвижения
- Опасные участки льда
- Таяние льда в водоёмах.
- Как определить толщину для рыбалки?
- Какой должна быть минимальная толщина покрова?
- Количество теплоты
- При какой температуре образуется снег?
- Фазовые переходы: изменение агрегатных состояний вещества
- Свойства
- Плавление льда
- Удельная теплота плавления и кристаллизации
Замерзание водоёмов
При интенсивном теплообмене и охлаждении вод водоема, но при отсутствии ветра и перемешивания верхних слоем воды образуются первичные кристаллики льда в виде мелких иголочек. Когда вода покрыта ими, кажется, что на её поверхности разлит растопленный жир. Такое состояние водно- кристаллизованной смеси называют «сало». При продолжающемся морозе и безветрии кристаллики смерзаются. Образуется однородный прозрачный кристаллический лед, толщина которого довольно быстро увеличивается. За ясную и морозную ночь толщина такого льда может достичь 2-3 см. При этом, как правило, весь небольшой водоём замерзает единовременно. На крупных озёрах в такую погоду обычно покрываются льдом только мелководные заливы.

Кристаллический лёд в начале зимы наиболее прочный и при толщине 5 см выдерживает вес человека, а при 10 см — снегохода. В озёрах, покрывшихся льдом в морозную, штилевую погоду, подо льдом сохраняется обратная стратификация с относительно тонким подлёдным слоем воды, охлажденной до 0 °С. Если замерзание водоёма происходило в ветреную погоду с перемешиванием и более интенсивной теплоотдачей с водной поверхности, средняя температуры воды в водоеме зимой меньше.
При даже слабом ветре замерзание водоёма начинается с береговых отмелей, выхолаживающейся быстрее из-за малой глубины. Первичные кристаллики сбиваются к урезу и смерзаются, образуя полосы кристаллического льда — забереги, примёрзшие к береговому склону. С усилением мороза забереги расширяются, а открытая поверхность воды сокращается. На крупных и глубоких озёрах и водохранилищах замерзание длительно и проходит разновременно в разных районах.
В формировании ледяного покрова принимают участие всплывающие комья внутриводного льда (шуга) обычно грязно-белого цвета, снежура, образующаяся из снега во взволнованной, ещё не замерзшей водной поверхности. Неровность такого покрова увеличивается, если сильный ветер и колебания поверхности водоёма взламывают ещё не окрепший лед. Он дробится, и трущиеся друг о друга его кусочки превращаются в блинчатый лёд — дискообразные льдинки с выпуклым белым краем смерзшихся ледяных крошек.

Штормовым ветром взламывается и уже достаточно прочный лёд, льдины надвигаются одна на другую и смерзаются в торосы с наступлением менее ветреной, но морозной погоды. На нагонных участках пологого берега из битого льда, шуги и частиц донного грунта в шторм образуются береговые ледяные валы.

Свойства
Основная масса бесцветна. Совсем прозрачный лёд характерен для пресноводных водоемов. Ярчайший пример — лёд на озере Байкал. Намерзшие глыбы абсолютно чистые и прозрачные. Морской и речной обычно имеют белый цвет с легким синеватым оттенком, а речной также имеет — грязный серый цвет, к тому же такие льды быстро тают.
Цвет льда напрямую зависит от окружающей обстановки. Так, лёд в воде кажется синим, потому что принято считать, что вода имеет именно такой оттенок.
Следующее свойство — блеск, похожий на стекло. Он также может порезать кожу человека. Основные массы не имеют спаек, вода буквально замерзает в монолитную массу без швов.

Минерал насчитывает более 14 модификаций, уже приведенных выше. На Земле встречается только два первых вида. Связано это с экстремально низкими температурами и высоким давлением, что свойственно другим планетам. Температура льда также может различаться: на вершинах гор она равна 0 градусов, тогда как самыми теплыми являются гренландские — 28 градусов.
Другая особенность — расширение массы замерзающий воды при образовании кристаллической решетки. Именно это свойство спасает флору и фауну во время зимы, не позволяя промерзать водоемам до самого дна. Возможно образование сосулек — длинных ледяных полотен до самого дна, но они никак не влияют на окружение.
Уникальность талой воды также не заканчивается на молекулярном уровне. Так, к примеру, талая вода будет довольно чистой и пригодной для питья. Поскольку образование льда является естественным очистителем для воды.
Существуют планеты, которые полностью покрывает горячий лед (например, Gliese 436 b). Разумеется, всё на уровне предположений — никто достоверно не знает. Предположительная температура на приведенной планете держится в 300°C, но сила давления настолько высока, что воду попросту сжимает и удерживает в твердом состоянии.
Различается удельная теплоемкость воды и льда в зависимости от температуры в интервале от 0 до -100°C. Снижение приводит к тому, что параметр значительно уменьшается, но теплопроводность и плотность, напротив, возрастает. Теплоемкость льда меньше в два раза, чем у воды, потому он может оставаться холодным, даже при высоких температурах (пример — гренландские теплые льды). Но их плотность будет близка к массе воды.
| Температура, °С | Плотность, кг/м3 | Теплопроводность, Вт/(м·град) | Теплоемкость, Дж/(кг·град) |
| 0.01 (Вода) | 999,8 | 0,56 | 4212 |
| 916,2 | 2,22 | 2050 | |
| -5 | 917,5 | 2,25 | 2027 |
| -10 | 918,9 | 2,30 | 2000 |
| -15 | 919,4 | 2,34 | 1972 |
| -20 | 919,4 | 2,39 | 1943 |
| -25 | 919,6 | 2,45 | 1913 |
| -30 | 920,0 | 2,50 | 1882 |
| -35 | 920,4 | 2,57 | 1851 |
| -40 | 920,8 | 2,63 | 1818 |
| -50 | 921,6 | 2,76 | 1751 |
| -60 | 922,4 | 2,90 | 1681 |
| -70 | 923,3 | 3,05 | 1609 |
| -80 | 924,1 | 3,19 | 1536 |
| -90 | 924,9 | 3,34 | 1463 |
| -100 | 925,7 | 3,48 | 1389 |
Таким образом, свойства льда не изучены в полной мере и могут предполагаться в лабораторных условиях.

Лёд и его разновидности
Существует дополнительная градация по разновидностям:
- атмосферный — твердый вид атмосферных осадков (снег, иней, град и даже туман);
- ледяная вода — также разновидность минерала, поскольку в неё присутствуют кристаллы;
- водяной покров — в воде, на её поверхности или прямо в массе (донный, внутриводный, ледяной);
- подземный — первичный и вторичный, относится к многолетним и вечным типам;
- ледниковый, соответственно, ледник.
Кроме того, разработан искусственный лёд. К нему также относятся разные типы поверхностей и разновидностей. Например, хоккейный лёд — специальное покрытие, максимально подходящее для игры. Сюда же относится материал покрытия для конькобежных видов спорта, фигурного катания и т.д.
Существует другая, сублимированная формула льда (CO2 — диоксид углерода), которая позволяет миновать жидкую фазу и сразу перейти в водяной пар. Таким образом достигается охлаждение пищевых продуктов, проводятся испытания и лабораторные исследования. Называется разновидность — синтетический или же сухой лёд.
Существует ещё много разновидностей: от цветного до обычного кубического льда, который легко делается в холодильнике.

Морфология
Природный лёд — это минерал, имеющий массу разновидностей. Часто это естественное скопление мелких частиц, перешедших из фазы жидкости. Но есть и виды, образованные вследствие сублимации. В целом, это масса, а именно кристаллы встречаются редко — сталактиты, сталагмиты. Наиболее яркий пример — Кунгурская ледяная пещера.
Ледяные забереги — полосы покрова, который образуется на границе между водой и воздухом. При этом основная часть воды не промерзает. Однако, начинаясь от берегов, они могут полностью срастаться на середине водоема, образуя сплошное полотно. Объем льда при этом может достигать как нескольких см, так и много метров.

Модель строения воды
Молекула воды включает два атома водорода (Н) и один атом кислорода (О). Элементы, из которых состоит жидкость, определяют всю функциональность и особенности. Модель молекулы воды имеет форму треугольника. Вершину этой геометрической фигуры представляет крупный элемент кислорода, а внизу находятся небольшие атомы водорода.
Молекула воды обладает двумя положительными и двумя отрицательными полюсами зарядов. Отрицательные заряды формируются из-за излишка электронной плотности у атомов кислорода, а положительные – из-за нехватки электронной плотности у водорода.
![]()
Неравномерное распределение электрических зарядов создает диполе, где диполярный момент составляет 1,87 дебай. Вода обладает способностью растворять вещества, поскольку ее молекулы пытаются нейтрализовать электрическое поле. Диполя приводят к тому, что на поверхности погруженных в жидкость веществ становятся слабее межатомные и межмолекулярные связи.
Вода отличает большой устойчивостью при растворении прочих соединений. В обычных условиях из 1 млрд молекул только 2 распадаются, а протон переходит в строение иона гидроксония (образуется при растворении кислот).
Вода не меняет свой состав при взаимодействии с другими веществами и не влияет на структуру этих соединений
Такая жидкость считается инертным растворителем, что особо важно для живых организмов. Полезные вещества поступают к различным органам через водные растворы, поэтому важно, чтобы их состав и свойства оставались неизменными
Вода сохраняет в себе память о растворенных в ней веществах и может применяться многократно.
Каковы особенности пространственной организации молекулы воды:
- Соединение проводится противоположными зарядами;
- Появляются межмолекулярные водородные связи, которые исправляют электронную неполноценность водорода с помощью дополнительной молекулы;
- Вторая молекула фиксирует водород по отношению к кислороду;
- Благодаря этому образуются четыре водородные связи, которые могут контактировать с 4 соседями;
- Такая модель напоминает бабочку и имеет углы равные 109 градусам.
Атомы водорода соединяются с атомами кислорода и образуют молекулу воды с ковалентной связью. Водородные соединения более сильные, поэтому, когда они разрываются, то молекулы присоединяются к другим веществам, способствуя их растворению.
Прочие химические элементы, в состав которых входит водород, замерзают при -90 градусах, а закипают при 70 градусах. Но вода становится льдом, когда температура достигает нуля, а закипает при 100 градусах. Чтобы объяснить такие отклонения от нормы, требуется разобраться, в чем особенность строения молекулы воды. Дело в том, что вода – это ассоциированная жидкость.
![]()
Это свойство подтверждается и большой теплотой парообразования, что делает жидкость хорошим энергоносителем. Вода – отличный регулятор температуры, способен нормализировать резкие перепады этого показателя. Теплоемкость жидкости повышается, когда ее температура 37 градусов. Минимальные показатели соответствуют температуре человеческого тела.
Относительная молекулярная масса воды составляет 18. Рассчитать этот показатель достаточно легко. Следует заранее ознакомиться с атомной массой кислорода и водорода, которая равна 16 и 1 соответственно. В химических задачах нередко встречается массовая доля воды. Этот показатель измеряется в проценте и зависит от формулы, которую требуется рассчитать.
Структура и деформации ледяною покрова.
Ледостав – период неподвижного ледяного покрова. В Ладожском озёре в теплую зиму с малой суммой отрицательных температур воздуха площадь ледяного покрова не превышает 50% площади акватории. В такие зимы теплозапас его водной массы наименьший вследствие особенно интенсивной теплоотдачи с большой открытой водной поверхности. В умеренно холодные зимы почти 100 %-ная покрытость льдом продолжается всего 2 месяца, а в суровые зимы она длится почти 3 месяца.
Скорость нарастания кристаллического слоя льда (вследствие кристаллизации воды на его нижней поверхности) зависит от его теплопроводности и того, насколько интенсивны теплопотери с ледяного покрова в атмосферу при морозе. Чем ниже температура воздуха и продолжительнее морозная погода, тем больше намерзает льда снизу, тем всё более толстым становится кристаллический лед на водоёме, увеличивается теплоизоляция воды под ним.
Как правило, ледяной покров неоднороден и имеет двух- или трёхслойную структуру и покрыт слоем снега неравномерной толщины и плотности. Под весом снега лёд прогибается, трескается, из трещин, рыбацких лунок и майн на лёд вытекает вода, смачивает нижний слой снега и в мороз замерзает. Так образуется водно-снеговой лёд, менее плотный и малопрозрачный белёсого цвета из-за включения пузырьков воздуха и пыли.
В оттепели талая вода с подтаивающего снежного покрова в последующие морозы превращается в снеговой лёд. Он по физическим свойствам сходен с водно-снеговым льдом, но отличается по химическому составу, подобному составу атмосферных осадков. Лёд этих двух видов имеет меньшую теплопроводность и отражающую способность, чем кристаллический лёд, что замедляет утолщение ледяного покрова.
Правильное хранение сухого льда
От того, как производится хранение льда, зависит, сколько он проживет. При покупке необходимо учитывать, что в день улетучивается около 3 кг субстанции. Лучшим вариантом станет приобретение льда незадолго до момента применения.
Хранить сухой лед рекомендуется в изолированных контейнерах: пенопластовом кулере, который не пропускает тепло извне, или стандартной сумке-холодильнике. Это позволит максимально длительное и удобное хранение дома.
Советы для использования контейнеров:
- Емкость должна быть полностью закрыта и иметь максимально толстые стенки. Это главное условие, так как из-за взаимодействия с теплым воздухом лед будет быстрее испаряться.
- Использование смятой бумаги позволит уменьшить процесс сублимации. Класть ее необходимо в оставшееся пустое пространство контейнера.
- Температуру снаружи емкости нужно поддерживать максимально низкой. Допустим, в холодное время года ее можно ставить на улицу, а в жаркое – на балкон или сарай, если он достаточно затемнен и прохладен.
Соблюдение данных рекомендаций позволит снизить расход сухого льда и не задаваться постоянным вопросом «сколько его еще осталось».
Как определить толщину для рыбалки?
Есть несколько способов, позволяющих проверить толщину льда на водоеме самостоятельно и обезопасить себя от проваливания под воду.
Проверяется лед палкой следующим образом: постучите по замерзшей поверхности и проследите за появлением воды. Если вода на поверхности появилась, лед еще не успел достаточно замерзнуть и ходить по нему совсем небезопасно. Уходить с тонкого льда стоит определенным образом: передвигайтесь медленно, ни в коем случае не паникуйте и не делайте слишком резких движения, ступни ног должны скользить по поверхности и не отрываться.
Еще один способ определения толщины – цвет льда. Самым крепким и безопасным считается прозрачный лет. Если поверхность имеет синеватый или зеленоватый оттенок, вставать на такой лед можно – толщина достигла минимально допустимых безопасных значений.
Самым небезопасным считается матовый лед имеющий желтоватый оттенок, он очень быстро разрушается, хождение по такой поверхности может обернуться плачевными последствиями.
Избегать стоит и участков льда, на котором нет никаких следов. Если в данном месте до сих пор никто не ходил, скорее всего, толщина недостаточная.
Правила передвижения
- переходя водоем, старайтесь придерживаться тех участков, где тропа уже протоптана. Вступая на чистый лед без следов, обязательно прощупывайте поверхность перед собой палкой;
- если вы рыбачите группой, стоит распределиться друг от друга на некотором расстоянии;
- передвигаться до места бурения лунок желательно на лыжах;
- если с собой вы взяли рюкзак со снаряжением, носить его стоит только на одной лямке. Это позволит в случае проваливания под лед быстро отбросить груз в сторону;
- обязательно берите на рыбалку с собой веревку, оптимальная длина – 20-25 метров. На один конец веревки привязывается груз и делается петля. Это позволяет оказать помощь провалившемуся под лед рыбаку в случае необходимости.
Желательно на зимнюю рыбалку не ходить самостоятельно
Важно также предупредить близких о том, в каком именно месте вы планируете рыбачить
Опасные участки льда
- Наибольшую опасность лед представляет поздней осень и ранней весной. В первом случае он еще не окреп, а во втором начинает таять;
- Не стоит передвигаться по льду, покрытому большим количеством снега, так как понять толщину под слоем снега нереально;
- Опасность представляют полыньи и рыбацкие лунки, не заметив их вы можете провалиться под лед;
- Лед на берегу значительно толще чем на середине водоема;
- На болотах лед, как правило, тонкий, он подогревается газами, которые находятся на болотах;
- В моменты повышения температур, не стоит отправляться на рыбалку, лед становится рыхлым хрупким, из полупрозрачного голубого превращается в белый.

Таяние льда в водоёмах.
Разрушение ледяного покрова, т. е. вскрытие замерзашего водоема, включает три стадии:
I стадия – таяние снежного покрова. Талая вода пропитывает снег, он темнеет, снижается величина отражающей способности поверхности водоёма, увеличивается поглощение суммарной солнечной радиации, что ускоряет таяние. Вода накапливается на льду, протаивают вдольбереговые трещины, заполняющиеся талой водой. Увеличение расхода воды в притоках приводит к подъему уровня воды в водоёме. Ледяной покров, освободившийся от снега, всплывает. Талая вода с него уходит под лёд. Вдоль берегов образуются закраины у скалистых крутых берегов и более широкие – на мелководьях.
II стадия – активное таяние ледяного покрова. Оно происходит на его верхней поверхности вследствие поглощения льдом солнечной радиации (большая величина радиационного баланса) и турбулентного теплообмена с более тёплым воздухом.
Подтаивает и нижняя поверхность льда вследствие конвективного перемешивания подлёдной воды с нижележащим слоем, нагретым днем проникающей сквозь лед солнечным излучением. Локально оно интенсифицируется динамическим перемешиванием в приустьевых зонах, куда поступают воды притоков. Плотностные течения, несущие теплоту и распространяющиеся из этих зон в подледном слое из-за малой минерализации и плотности вод речного половодья, усиливают подтаивание снизу ледяного покрова. Стаивание льда сверху и снизу уменьшает толщину ледяного покрова примерно на 30 %.
Одновременно таяние происходит внутри пористого водноснегового и прозрачного кристаллического слоев. Оно начинается вокруг содержащихся во льду частиц ионного состава. Образующиеся капли внутрилёдной солоноватой талой воды, поглощающие солнечное излучение, вызывают протаивание вертикальных канальцев диаметром 0,1-1,0 мм между ледяными кристаллами. Это увеличивает рассеяние и поглощение солнечного света в толще льда и ускоряет таяние. Канальца расширяются до 5 мм и более в диаметре, и внутрилёдная вода стекает под лёд, происходит его обессоливание.
Прочность ледяного поля уменьшается настолько, что любая даже небольшая на него нагрузка – ветровое пульсирующее давление сверху или сейшевые колебания воды снизу – разрывает ослабевшие связи между кристаллами льда. Лед рассыпается на отдельные кристаллы диаметром до 5-7 см и длиной 20-30 см и более. В эту стадию выход на лёд крайне опасен.
III стадия – таяние возникающих полей ледяных иглообразных кристаллов и еще не раздробленных льдин. Оно происходит обычно быстро благодаря резкому снижению альбедо смеси воды и ледяных кристаллов, их механическому дроблению волнением и трением друг о друга. Из-за поглощения льдом солнечного излучения весной для его таяния и разрушения в водоёме достаточна в 5 раз меньшая сумма положительных температур воздуха, чем сумма её отрицательных значений зимой для формирования толщи ледяного покрова.
Вскрытие малых озёр, прудов и водохранилищ происходит практически одновременно на всей их акватории. В целом сроки начала ледостава и очищения ото льда озёр и водохранилищ – более поздние, чем на реках. Их запаздывание тем значительнее, чем больше размеры водоёма и меньше его проточность.
Источник
Как определить толщину для рыбалки?
Есть несколько способов, позволяющих проверить толщину льда на водоеме самостоятельно и обезопасить себя от проваливания под воду.
Проверяется лед палкой следующим образом: постучите по замерзшей поверхности и проследите за появлением воды. Если вода на поверхности появилась, лед еще не успел достаточно замерзнуть и ходить по нему совсем небезопасно. Уходить с тонкого льда стоит определенным образом: передвигайтесь медленно, ни в коем случае не паникуйте и не делайте слишком резких движения, ступни ног должны скользить по поверхности и не отрываться.
Еще один способ определения толщины – цвет льда. Самым крепким и безопасным считается прозрачный лет. Если поверхность имеет синеватый или зеленоватый оттенок, вставать на такой лед можно – толщина достигла минимально допустимых безопасных значений.
Самым небезопасным считается матовый лед имеющий желтоватый оттенок, он очень быстро разрушается, хождение по такой поверхности может обернуться плачевными последствиями.
Избегать стоит и участков льда, на котором нет никаких следов. Если в данном месте до сих пор никто не ходил, скорее всего, толщина недостаточная.
Какой должна быть минимальная толщина покрова?
В большинстве регионов нашей страны рыбаки на лед выходят в случае, если толщина льда на водоеме превышает 7 сантиметров, при этом самым безопасным считается лед, толщина которого превышает 10 сантиметров.
Пешие переправы через водоем можно разрешить, если толщина льда превышает 15 сантиметров.
Санкционированная переправка транспорта по льду становится доступна только в том случае, если толщина превышает 30 сантиметров.
Стоит помнить о том, что лед одинаково толстый не во всех местах. Даже при достижении оптимальной толщины в центральной части водоема, возле берега, а также в районе слияния рек наблюдаются тонкие участки, представляющие опасность.
Количество теплоты

В такой науке, как физика, часто используется понятие количества теплоты. Данная величина показывает количество энергии, необходимой для нагревания, плавления, кристаллизации, кипения, испарения или конденсации различных веществ. Причем каждый из перечисленных процессов имеет свои особенности. Поговорим о том, какое количество теплоты для нагревания льда требуется в обычных условиях.
Чтобы нагреть лед, нужно сначала его растопить. Для этого необходимо количество теплоты, нужное для плавления твердого вещества. Теплота равняется произведению массы льда на удельную теплоту его плавления (330-345 тысяч Джоулей/кг) и выражается в Джоулях. Допустим, что нам дано 2 кг твердого льда. Таким образом, чтобы его растопить, нам понадобится: 2 кг * 340 кДж/кг = 680 кДж.
После этого нам необходимо нагреть образовавшуюся воду. Количество теплоты для данного процесса рассчитать будет немного сложнее. Для этого нужно знать начальную и конечную температуру нагреваемой воды.
Итак, допустим, что нам требуется нагреть получившуюся в результате плавления льда воду на 50 °C. То есть разница начальной и конечной температуры = 50 °C (начальная температура воды – 0 °C). Тогда следует умножить разность температур на массу воды и на ее удельную теплоемкость, которая равняется 4 200 Дж*кг/°C. То есть количество теплоты, необходимое для нагревания воды, = 2 кг * 50 °C * 4 200 Дж*кг/°C = 420 кДж.
Тогда получаем, что для плавления льда и последующего нагревания получившейся воды нам потребуется: 680 000 Дж + 420 000 Дж = 1 100 000 Джоулей, или 1,1 Мегаджоуль.
Зная, при какой температуре тает лед, можно решить множество непростых задач по физике или химии.
При какой температуре образуется снег?
Осадки выпадают в виде снега, когда температура воздуха ниже 2 °C. Существует миф, что для образования снега температура должна быть ниже ноля. На самом деле самые тяжелые снежинки выпадают уже при температуре между 0 и 2°C. Выпавший снег начинает таять, когда температура поднимается выше 0 °C, но как только происходит процесс таяния, температура воздуха в области нахождения снежных осадков начинает понижаться.
Если температура выше 2 °C, то снежинки начинают таять и выпадают, скорее всего, в виде мокрого снега, нежели в виде обычного снега. А если температура так и не понизится, то вместо снега пойдет дождь.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:

Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
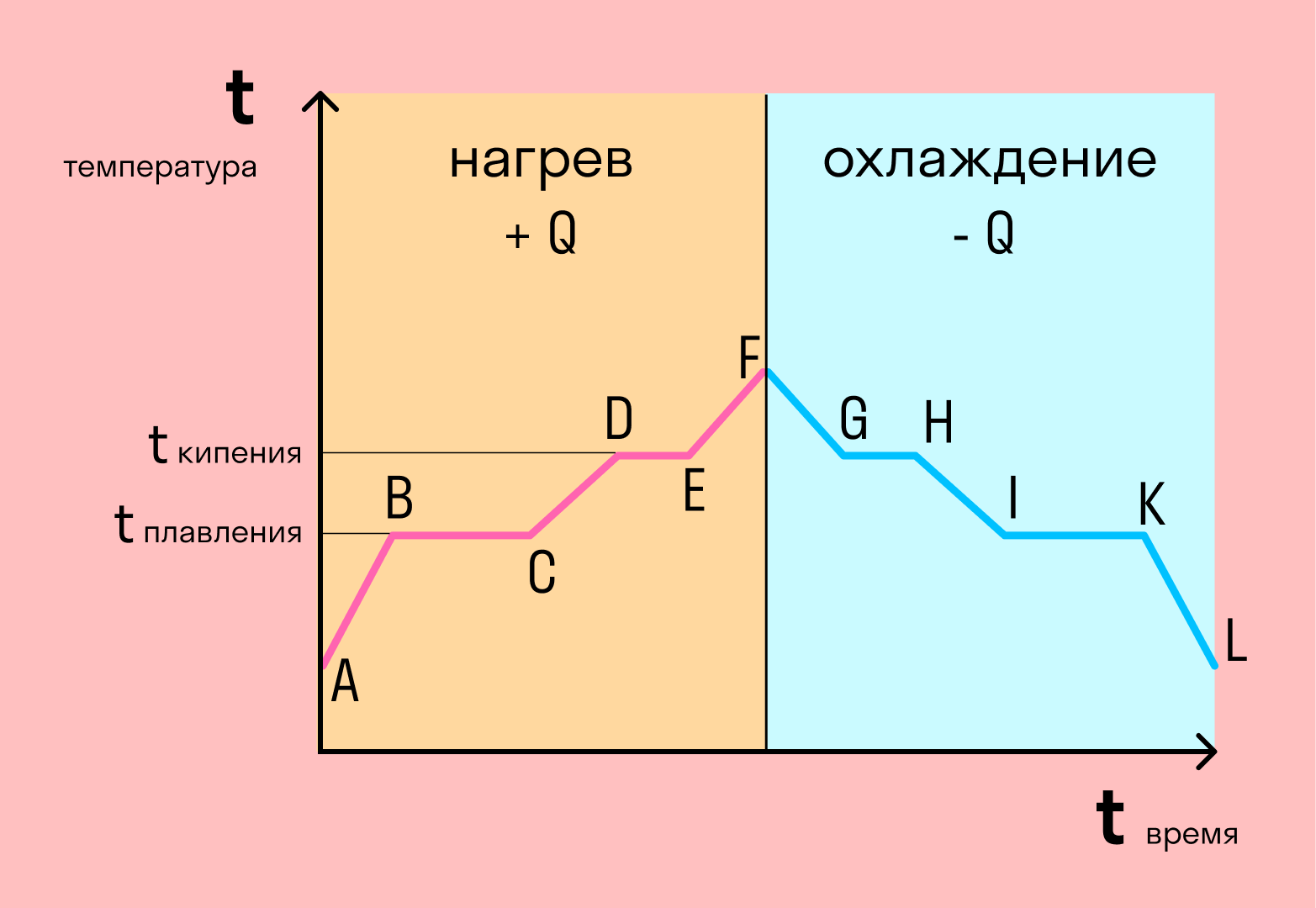
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
AB — нагревание льда
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
BC — плавление льда
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
CD — нагревание воды
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
DE — кипение (парообразование) воды
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
EF — нагревание пара
Первый шаг в обратную сторону — охлаждение до температуры кипения.
FG — охлаждение пара
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
GH — конденсация пара
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
HI — охлаждение воды
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
IK — кристаллизация воды
После кристаллизации лед охлаждается.
KL — охлаждение льда
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
|
Нагревание Q = cm(tконечная-tначальная) Охлаждение Q = cm(tначальная-tконечная)) Q — количество теплоты c — удельная теплоемкость вещества [Дж/кг*˚C] m — масса tконечная — конечная температура tначальная — начальная температура |
|
Плавление Q = λm Кристаллизация Q = — λm Q — количество теплоты λ — удельная теплота плавления вещества [Дж/кг] m — масса |
|
Парообразование Q = Lm Конденсация Q = — Lm Q — количество теплоты L — удельная теплота парообразования вещества [Дж/кг] m — масса |
Свойства
![]()
Текстура льда
Лёд бесцветен. В больших скоплениях он приобретает синеватый оттенок. Блеск стеклянный. Прозрачный. Спайности не имеет. Твердость 1,5. Хрупкий. Оптически положительный, показатель преломления очень низкий (n = 1,310, nm = 1,309). В природе известны 14 модификаций льда. Правда, все, кроме привычного нам льда, кристаллизующего в гексагональной сингонии и обозначающегося как лёд I , образуются в условиях экзотических — при очень низких температурах (порядка -110150 0С) и высоких давлениях, когда углы водородных связей в молекуле воды изменяются и образуются системы, отличные от гексагональной. Такие условия напоминают космические и не встречаются на Земле.
Например, при температуре ниже –110 °С водяные пары выпадают на металлической пластине в виде октаэдров и кубиков размером в несколько нанометров — это так называемый кубический лед. Если температура чуть выше –110 °С, а концентрация пара очень мала, на пластине формируется слой исключительно плотного аморфного льда.
Плавление льда

В природе твердый лед существует только при температуре 0 °C и ниже. Если же температура окружающей среды поднимается и становится больше 0 °C, лед начинает таять.
При температуре таяния льда, при 0 °C, происходит и другой процесс – замерзание, или кристаллизация, жидкой воды.
Данный процесс можно наблюдать всем жителям умеренно континентального климата. Зимой, когда температура на улице опускается ниже 0 °C, достаточно часто выпадает снег, который не тает. А жидкая вода, находившаяся на улицах, замерзает, превращаясь в твердый снег или лед. Весной же можно увидеть обратный процесс. Температура окружающей среды поднимается, поэтому лед и снег тают, образуя многочисленные лужи и грязь, которую можно считать единственным минусом весеннего потепления.
Таким образом, можно сделать вывод, что, при какой температуре начинает таять лед, при такой же температуре начинается и процесс замерзания воды.
Удельная теплота плавления и кристаллизации
Как определить количество теплоты, которое должно поглотить твердое кристаллическое тело массой т, чтобы перейти в жидкое состояние, т. е
расплавиться? Еще раз обращаем ваше внимание на то, что температура во время плавления не изменяется (см. рис
50, участок ВС), но теплота телу сообщается. Значит, она идет на разрушение кристаллической упорядоченной структуры вещества тела.
Физическая величина, численно равная количеству теплоты, которое необходимо передать твердому телу массой 1 кг при температуре плавления для перехода в жидкое состояние, называется удельной теплотой плавления.
Удельная теплота плавления обозначается греческой буквой (ламбда).
Чтобы расплавить твердое тело массой 2 кг, ему надо передать энергии (теплоты) Q в 2 раза больше. А если масса тела равна m? Очевидно, для перехода в жидкое состояние тело должно получить теплоты Q в m раз больше, т. е.
Из этой формулы следует, что удельная теплота плавления определяется как
В СИ единицей удельной теплоты плавления является 1 джоуль на килограмм
У различных веществ удельная теплота плавления неодинакова. В таблице 3 приведены ее значения для разных веществ. Как следует из таблицы, для ртути равна 11800 5 Это значит, что для перехода ртути массой m = 1 кг, имеющей температуру t = -39°С, из твердого состояния в жидкое ей надо передать Q = 11 800 Дж энергии. Больше всего теплоты для плавления массы m = 1 кг требуется льду — (рис. 54, а). Но при замерзании при температуре t = 0 °C столько же теплоты выделяет каждый килограмм воды (рис. 54, б).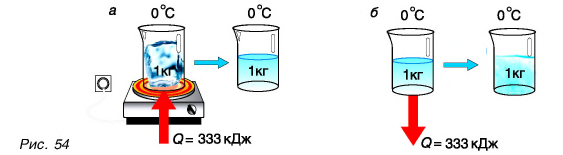
Большая удельная теплота плавления объясняет затяжное таяние льда озер, рек и других водоемов. А так как теплоту лед поглощает из окружающей среды, то погода в это время, как правило, прохладная. И наоборот, при замерзании озер, рек и других водоемов (рис. 55) выделяется большое количество энергии, что делает более теплой позднюю осеннюю погоду, а климат вблизи морей и океанов более умеренным.
Главные выводы:
- При переходе 1 кг вещества из твердого состояния в жидкое поглощается количество теплоты, численно равное удельной теплоте плавления, и ровно столько же теплоты выделяется при его переходе из жидкого состояния в твердое.
- Температуры плавления и кристаллизации для данного вещества одинаковы.
- Удельная теплота плавления у разных веществ различная.
Пример решения задачи
В горячую воду температурой опустили кубик льда массой = 0,20 кг, имеющий температуру Окончательная температура воды стала t = 20 °C. Определите массу горячей воды. Потерями теплоты пренебречь.
Дано:
Решение:
Составим уравнение теплового баланса: Отдавала теплоту горячая вода, охлаждаясь от температуры до температуры t: Лед получал теплоту, за счет которой он нагрелся от превратился в воду, затем полученная вода нагрелась от температуры до температуры t:
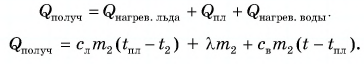
Тогда 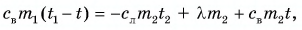
откуда
Ответ: = 0,3 кг.
| Рекомендую подробно изучить предметы: |
|
| Ещё лекции с примерами решения и объяснением: |
- Испарение жидкостей в физике
- Поверхностное натяжение жидкости
- Свойства паров в физике
- Кипение жидкостей в физике
- Инфракрасные излучения
- Количество теплоты в физике
- Расчет количества теплоты при нагревании и охлаждении
- Удельная теплота сгорания топлива